Chuyên đề nhận ra các hóa chất là dạng bài bác tập thân quen thường gặp gỡ trong công tác Hóa lớp 9, lớp 11 giỏi 12. Để giải những dạng bài bác tập nhận thấy các chất hóa học, yêu cầu học sinh cần cố chắc kiến thức cũng như các phương pháp giải. Bài viết dưới đây của phukiennail.net sẽ giúp đỡ bạn tổng hợp những kiến thức về nhà đề nhận biết các chất hóa học, cùng tìm hiểu nhé!.
Mục lục
1 chuyên đề nhận ra các hóa chất lớp 93 phương pháp nhận biết các chất vô cơ4 phương pháp nhận biết các chất hóa học hữu cơ lớp 115 Bảng phân biệt các chất hóa học lớp 8Chuyên đề phân biệt các hóa chất lớp 9
Nguyên tắc cùng yêu cầu khi giải bài tập dấn biết
Để riêng biệt hay nhận thấy các chất hóa học, ta cần phụ thuộc vào phản ứng đặc trưng và coi xét những hiện tượng: Như tất cả chất kết tủa sản xuất thành sau phản ứng, việc đổi color dung dịch, giải phóng chất bám mùi hoặc có hiện tượng kỳ lạ sủi bọt bong bóng khí. Hoặc để nhận ra các hóa học hóa học, bạn có thể sử dụng một số trong những tính chất vật lí (nếu như bài bác cho phép) như nung ở nhiệt độ khác nhau, tốt hoà tan những chất vào nước…Phản ứng hoá học tập được lựa chọn để nhận thấy là bội nghịch ứng sệt trưng đơn giản và dễ dàng và có dấu hiệu rõ rệt. Trừ ngôi trường hợp đặc biệt, thông thường muốn phân biệt n hoá chất nên phải triển khai (n – 1) thí nghiệm.Tất cả các chất được lựa chọn dùng để làm nhận biết những hoá hóa học theo yêu cầu của đề bài, các được coi là thuốc thử.Bạn đang đọc: Nhận biết các chất hóa học lớp 11
***Lưu ý: Khái niệm phân biệt bao hàm ý đối chiếu (ít độc nhất phải gồm hai hoá hóa học trở lên) tuy vậy mục đích sau cùng của sáng tỏ cũng là nhằm nhận biết tên của một số trong những hoá chất nào đó.Phương pháp giải bài xích tập nhận ra các chất hóa học
Bước 1: Đầu tiên buộc phải chiết (trích mẫu mã thử) những chất cần nhận ra vào các ống nghiệm (có tấn công số ráng thể).Bước 2: chọn thuốc thử phù hợp (tuỳ theo yêu cầu đề bài: thuốc test tuỳ chọn, hạn chế hay là không dùng thuốc thử nào khác).Bước 3: cho vào những ống nghiệm ghi nhận những hiện tượng, tiếp nối rút ra kết luận đã nhận biết, phân minh được hoá chất nào.Bước 4: Viết PTHH minh hoạ.
Các dạng bài xích tập hay gặp
Dạng 1: nhận biết hoặc phân biệt các hoá hóa học (rắn, lỏng, khí) riêng biệt biệt.Dạng 2: nhận ra hoặc phân biệt các chất trong cùng một hỗn hợp.Dạng 3: xác minh việc có mặt của các chất (hoặc các ion) trong và một dung dịch.Tuỳ theo yêu cầu của bài xích tập mà trong những dạng tất cả thể chạm mặt 1 trong những trường vừa lòng sau:
Nhận biết với dung dịch thử thoải mái (tùy chọn).Nhận biết với thuốc thử tinh giảm (có giới hạn).Nhận biết không được dùng thuốc thử mặt ngoài.Phương pháp nhận thấy các chất vô cơ
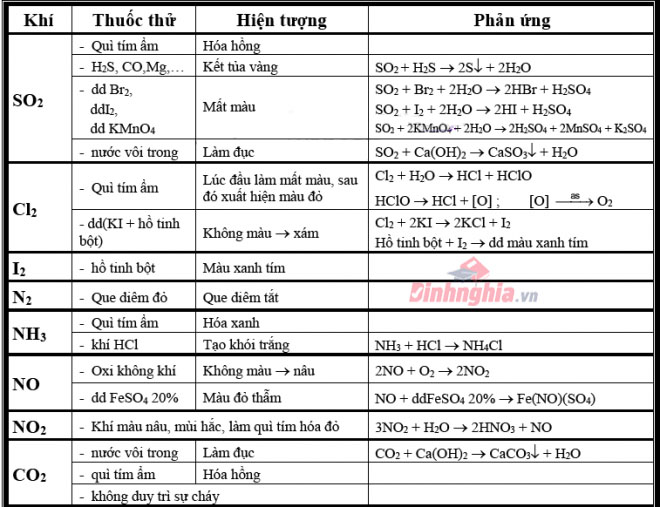
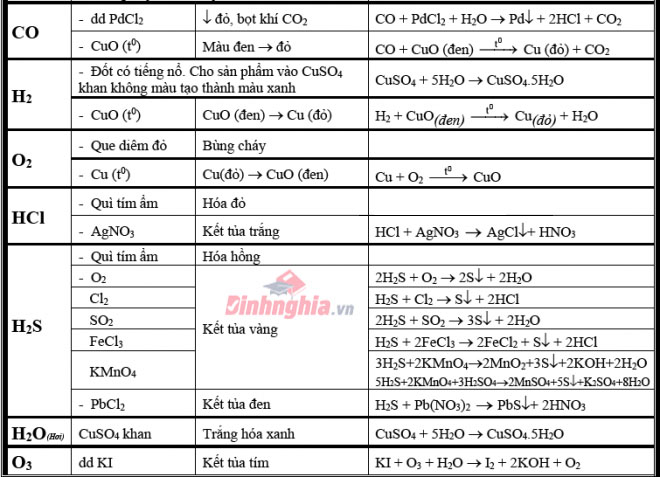
Đối với hóa học khí
Khí (CO_2): sử dụng dung dịch nước vôi trong gồm dư, hiện tượng xảy ra là có tác dụng đục nước vôi trong.Khí (SO_2): bám mùi hắc nặng nề ngửi, có tác dụng phai màu hoả hồng hoặc làm mất đi màu dung dịch nước Brôm hoặc làm mất màu dung dịch thuốc tím.(5SO_2 + 2KMnO_4 + 2H_2O ightarrow 2H_2SO_4 + 2MnSO_4 + K_2SO_4)Khí (NH_3): có mùi khai, làm cho quỳ tím tẩm ướt hóa xanh.Khí Clo: sử dụng dung dịch KI + hồ tinh bột để thử clo làm cho dung dịch từ màu trắng chuyển thành màu xanh.(Cl_2 + KI ightarrow 2KCl + I_2)Khí (H_2S): nặng mùi trứng thối, cần sử dụng dung dịch (Pb(NO_3)_2) để tạo thành thành PbS kết tủa màu sắc đen.Khí HCl: làm giấy quỳ tẩm ướt hoá đỏ hoặc sục vào hỗn hợp (AgNO_3) sản xuất thành kết tủa white color của AgCl.Khí (N_2): Đưa que diêm đỏ vào có tác dụng que diêm tắt.Khí NO (không màu): Để ngoài không khí hoá màu nâu đỏ.Khí (NO_2) (màu nâu đỏ): mùi hắc, có tác dụng quỳ tím tẩm ướt hoá đỏ.(4NO_2 + 2H_2O + O_2 ightarrow 4HNO_3)Nhận biết dung dịch bởi quỳ tím
Để cần sử dụng quỳ tím nhận biết các chất, ta cần để ý như sau:
Nhận biết dung dịch bazơ (kiềm): làm cho quỳ tím hoá xanhNhận biết dung dịch axit: làm cho quỳ tím hoá đỏNhận biết hỗn hợp bazơ
Nhận biết (Ca(OH)_2):Dùng (CO_2) sục vào đến khi xuất hiện kết tủa thì ngừng lại.Dùng (Na_2CO_3) để tạo thành thành kết tủa white color của (CaCO_3)Nhận biết (Ba(OH)_2):Dùng dung dịch (H_2SO_4) để tạo ra thành kết tủa màu trắng của (Ba_2SO_4)Nhận biết dung dịch axit
Dung dịch HCl: cần sử dụng dung dịch (AgNO_3) làm lộ diện kết tủa white color của AgCl.Dung dịch (H_2SO_4): dùng dung dịch (BaCl_2) hoặc (Ba(OH)_2) tạo nên kết tủa (BaSO_4).Dung dịch (HNO_3): cần sử dụng bột đồng đỏ với đun ở ánh sáng cao làm xuất hiện dung dịch màu xanh và bao gồm khí gray clolor thoát ra của (NO_2).Dung dịch (H_2S): cần sử dụng dung dịch (Pb(NO_3)_2) lộ diện kết tủa màu đen của PbS.Dung dịch (H_3PO_4): sử dụng dung dịch (AgNO_3) làm mở ra kết tủa màu kim cương của (Ag_3PO_4).Nhận biết các dung dịch muối
Muối clorua: sử dụng dung dịch (AgNO_3).Muối sunfat: áp dụng dung dịch (BaCl_2) hoặc (Ba(OH)_2).Muối cacbonat: thực hiện dung dịch HCl hoặc (H_2SO_4).Muối sunfua: sử dụng dung dịch (Pb(NO_3)_2).Muối phôtphat: áp dụng dung dịch (AgNO_3) hoặc dùng dung dịch (CaCl_2), (Ca(OH)_2) làm lộ diện kết tủa mùa trắng của (Ca_3(PO_4)_2).Nhận biết những oxit của kim loại
Hỗn vừa lòng oxit: Hoà chảy từng oxit vào nước (Bao gồm 2 nhóm: tan trong nước với không tung trong nước).
Nhóm chảy trong nước cho công dụng với (CO_2)Nếu không có kết tủa: kim loại trong oxit là kim loại kiềm.Nhóm không tan nội địa cho công dụng với hỗn hợp bazơ.Nếu oxit rã trong hỗn hợp kiềm thì kim loại trong oxit là Be, Al, Zn, Cr..Nếu oxit ko tan trong hỗn hợp kiềm thì kim loại trong oxit là kim loại kiềm thổ.Nhận biết một số oxit
((Na_2O; K_2O; BaO)) cho tác dụng với nước ( ightarrow) dd vào suốt, làm xanh quỳ tím.((ZnO; Al_2O_3)) vừa tính năng với dung dịch axit, vừa chức năng với dung dịch bazơ.CuO tan trong hỗn hợp axit tạo thành dung dịch có màu xanh da trời đặc trưng.(P_2O_5) cho tác dụng với nước( ightarrow) dung dịch làm cho quỳ tím hoá đỏ.(MnO_2) cho công dụng với dung dịch HCl đặc có khí màu quà xuất hiện.Nhận biết các chất kết tủa
Màu của một vài kết tủa thường xuyên gặp
(Al(OH)_3): kết tủa keo trắng.Xem thêm: Bao La Vùng Trời 2 - Vùng Trời Bao La Ii
FeS: kết tủa màu đen.(Fe(OH)_2): kết tủa trắng xanh.(Fe(OH)_3): kết tủa nâu đỏ.(FeCl_2): hỗn hợp lục nhạt.(FeCl_3): dung dịch vàng nâu.Cu: kết tủa là màu sắc đỏ.(Cu(NO_3)_2): dung dịch xanh lam.(CuCl_2): tinh thể tất cả màu nâu, dung dịch xanh lá cây.(Fe_3O_4) (rắn): màu nâu đen.(CuSO_4): tinh thể khan màu trắng, tinh thể ngậm nước greed color lam, hỗn hợp xanh lam.(Cu_2O): đỏ gạch.(Cu(OH)_2): kết tủa xanh xao (xanh domain authority trời).CuO: kết tủa color đen.(Zn(OH)_2): kết tủa keo trắng.(Ag_3PO_4): kết tủa vàng.AgCl: kết tủa màu sắc trắng.AgBr: kết tủa vàng nhạt.AgI: kết tủa tiến thưởng cam (hay xoàn đậm).(Ag_2SO_4): kết tủa trắng.(MgCO_3): kết tủa trắng.(CuS, FeS, Ag_2S, PbS, HgS): màu sắc đen.(BaSO_4): kết tủa trắng.(BaCO_3): kết tủa trắng.(CaSO_3): kết tủa trắng.(Mg(OH)_2): kết tủa color trắng.(PbI_2): kết tủa quà tươi.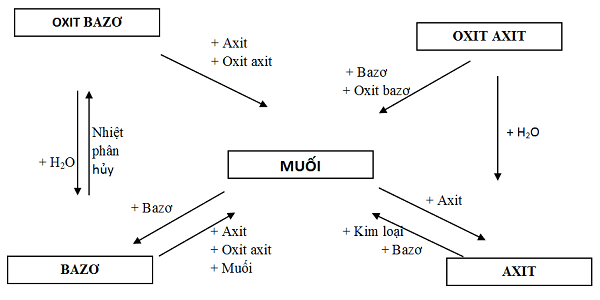
Phương pháp phân biệt các chất hóa học hữu cơ lớp 11
Với đề thi THPT non sông môn Hóa, dạng bài tập nhận biết các chất là dạng bài bác thường chạm chán và dễ dàng lấy điểm. Mỗi loại chất sẽ sở hữu những thuốc thử hay sử dụng khác nhau để phân biệt. Dưới đây là bảng phân biệt các hóa học hữu cơ tổng kết các thuốc thử thường xuyên dùng cũng giống như hiện tượng thu được khi nhận ra các hợp hóa học hữu cơ thường gặp.
Bảng phân biệt các chất hữu cơ tổng quát
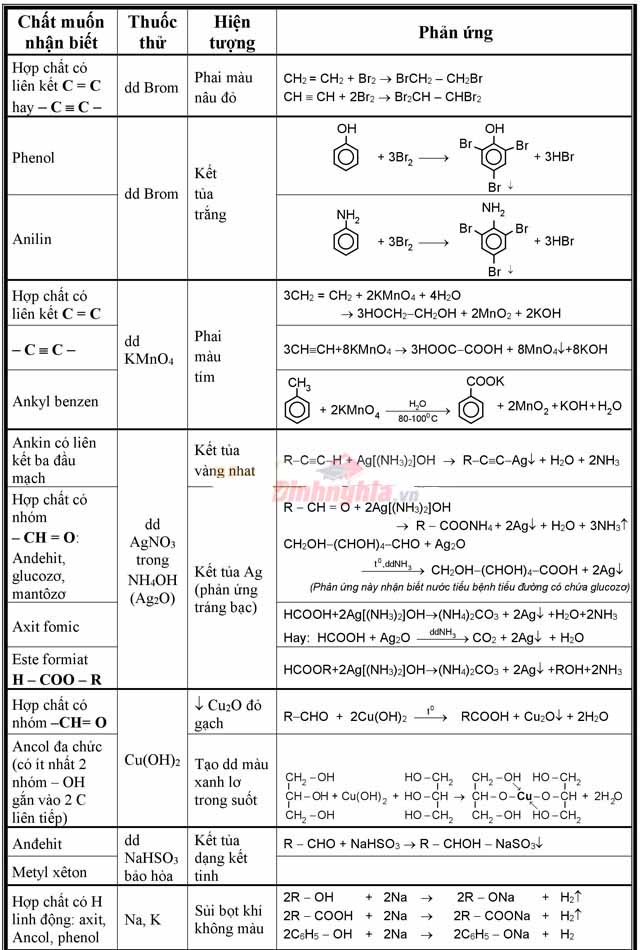
Bảng nhận ra các hóa học hữu cơ đưa ra tiết
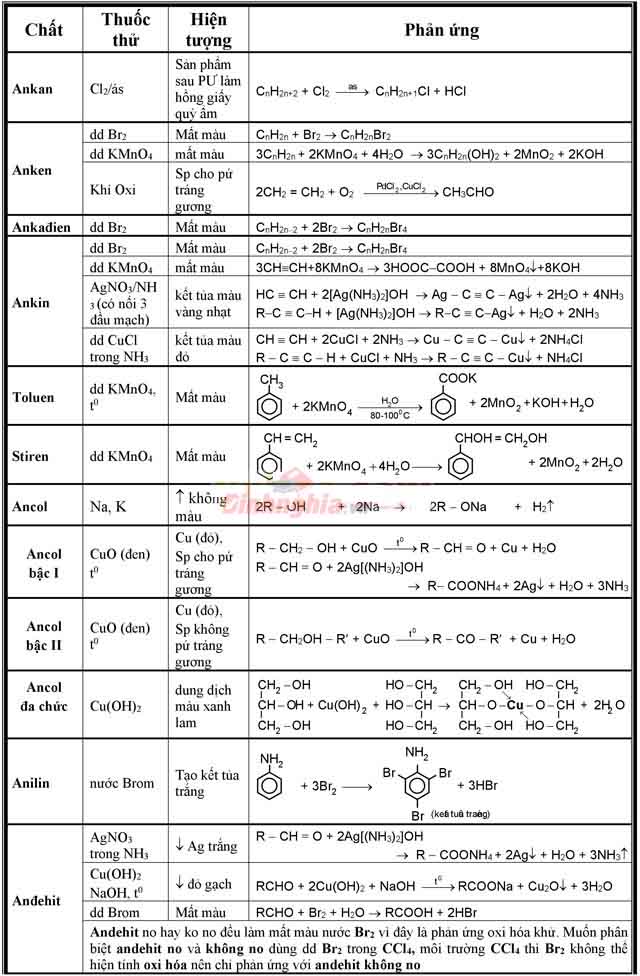
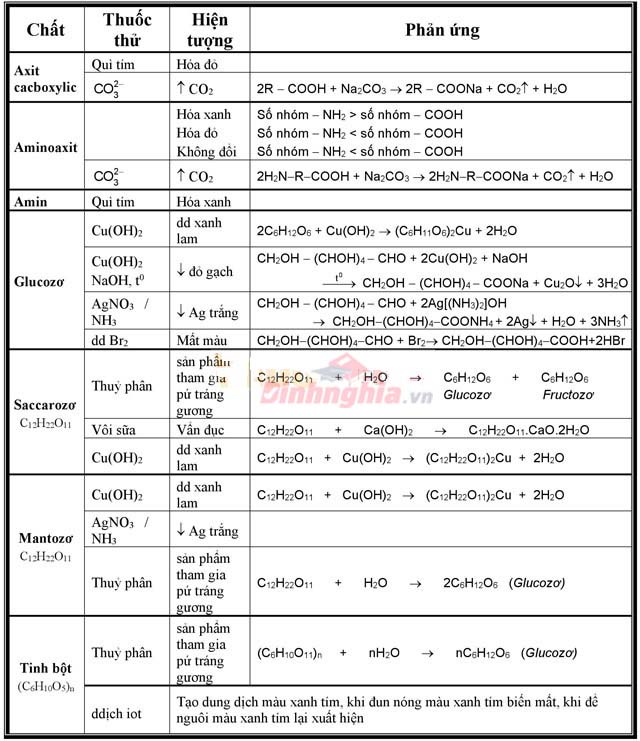
Bảng nhận ra các hóa chất lớp 8
Trạng thái, màu sắc các đối chọi chất, hòa hợp chất
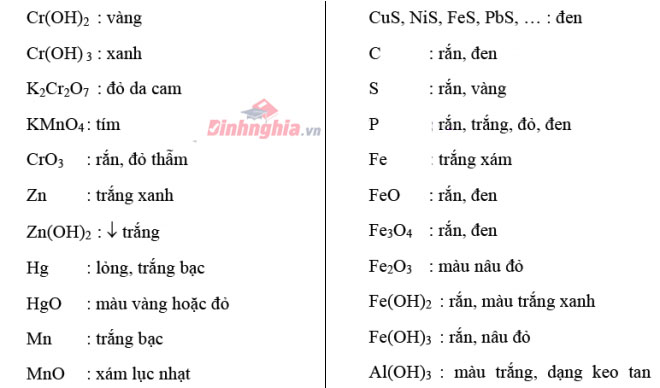

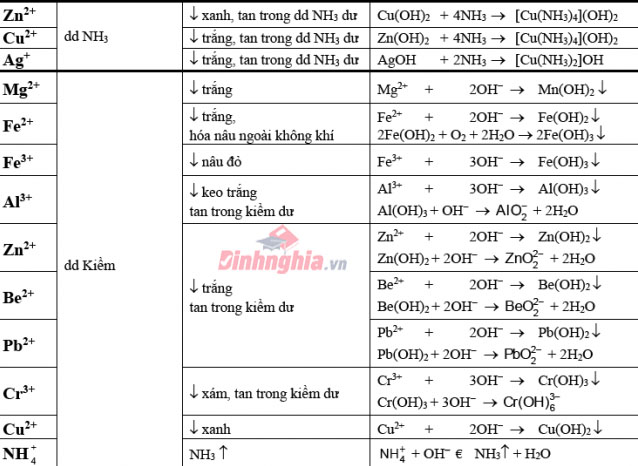
Bảng nhấn biết một số cation hay gặp
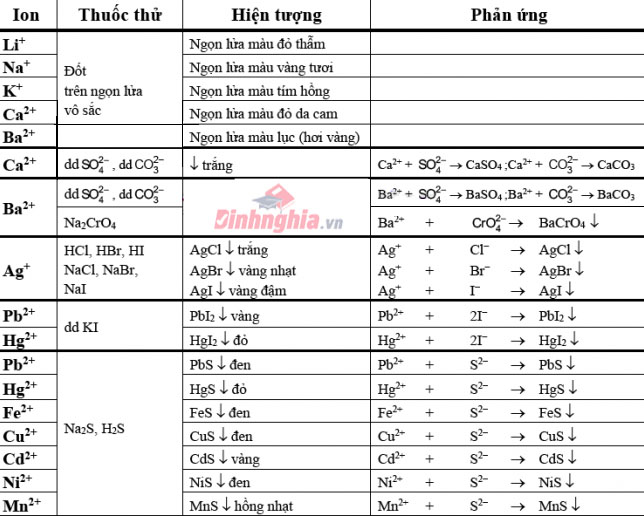
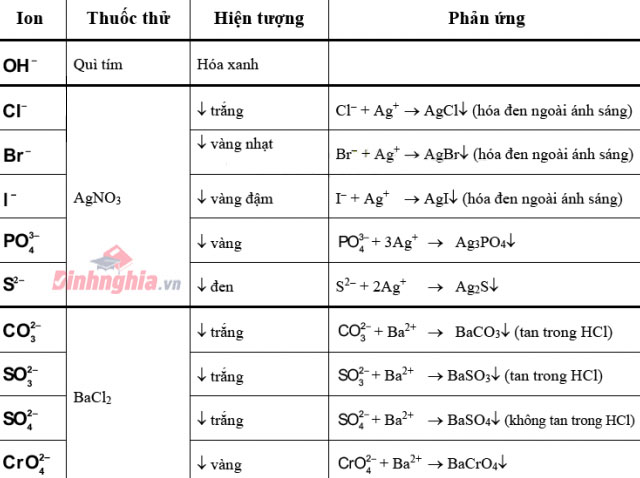
Bảng nhận biết một số trong những anion xuất xắc gặp
Như vậy, phukiennail.net đã giúp đỡ bạn tổng hòa hợp những kỹ năng và kiến thức hữu ích về công ty đề cách thức nhận biết những chất hóa học. Chúc bạn luôn luôn học tốt!.






